妇科腹腔镜器械临床前性能验证流程与标准解读
性能验证相关服务热线: 微析检测业务区域覆盖全国,专注为高分子材料、金属、半导体、汽车、医疗器械等行业提供大型仪器测试、性能测试、成分检测等服务。 地图服务索引: 服务领域地图 检测项目地图 分析服务地图 体系认证地图 质检服务地图 服务案例地图 新闻资讯地图 地区服务地图 聚合服务地图
本文包含AI生成内容,仅作参考。如需专业数据支持,可联系在线工程师免费咨询。
妇科腹腔镜器械在妇科诊疗领域发挥着极为重要的作用。本文将详细解读其临床前性能验证的流程与标准,涵盖从器械设计到各项关键性能指标验证等多方面内容,帮助相关人员深入了解确保这些器械安全有效投入临床使用的具体要求和规范。
一、妇科腹腔镜器械概述
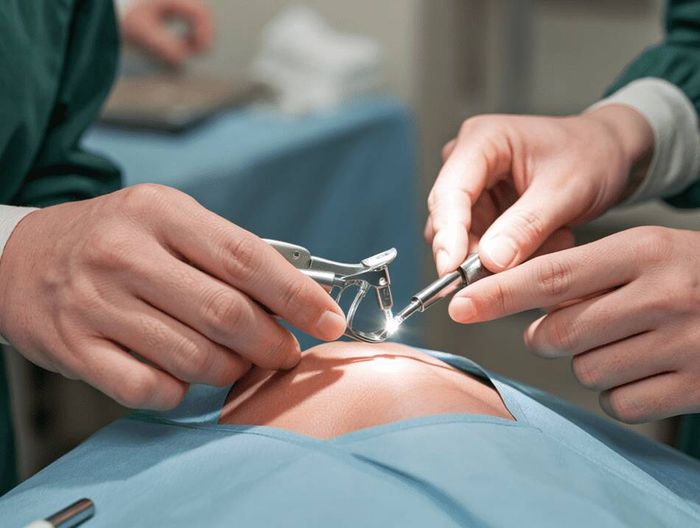
妇科腹腔镜器械是专门用于妇科腹腔镜手术的一系列工具。其种类繁多,包括腹腔镜镜头、穿刺器、分离钳、抓钳、电凝钩等。这些器械的设计目的在于通过微创的方式,协助医生清晰观察盆腔内的情况,并准确地进行各种手术操作,如切除病变组织、分离粘连等。与传统的开腹手术器械相比,妇科腹腔镜器械具有尺寸小巧、操作精准度要求高、能够在有限的腹腔空间内灵活施展等特点。例如腹腔镜镜头,它需要具备高清晰度的成像能力,以便医生能清晰辨别细微的组织结构;穿刺器则要保证在穿刺腹壁进入腹腔的过程中,既能顺利穿透又不会对周围组织造成过度损伤。
妇科腹腔镜器械的材质也至关重要。一般多采用医用不锈钢、钛合金等材料,这些材料具有良好的生物相容性、耐腐蚀性和机械强度。医用不锈钢材质的器械较为常见,其成本相对较低且易于加工制造;钛合金材质则在一些对器械轻便性和生物相容性要求更高的器械上应用,比如部分高端的腹腔镜抓钳等,能够更好地满足临床手术长时间操作的需求,减少患者因器械过重或材料反应而可能出现的不适。
二、临床前性能验证的重要性
临床前性能验证对于妇科腹腔镜器械来说意义重大。首先,它关乎患者的安全。在正式应用于临床手术之前,必须确保这些器械在正常使用情况下不会对患者的身体造成额外的伤害,比如器械的尖锐部分不会意外断裂遗留在患者体内,或者器械表面不会因材质问题导致患者过敏等不良反应。只有经过严格的性能验证,才能最大程度地降低手术风险,保障患者的生命健康。
其次,临床前性能验证有助于提高手术的成功率。准确有效的器械性能是医生顺利完成手术操作的重要保障。例如,若腹腔镜镜头的成像不清晰,医生就难以准确判断病变位置和周围组织关系,可能导致手术失误;若分离钳的夹持力不稳定,在分离粘连组织时就可能出现滑脱等情况,影响手术进程。通过验证器械的各项性能指标并使其达到标准要求,可以为医生提供可靠的手术工具,从而提高手术的精准度和成功率。
再者,规范的临床前性能验证也是医疗器械行业健康发展的需要。它促使生产企业不断改进产品设计和制造工艺,提高产品质量。只有符合严格验证标准的器械才能在市场上流通,这有利于淘汰那些质量不过关的产品,营造一个公平竞争、高质量发展的医疗器械市场环境。
三、验证流程的启动阶段
妇科腹腔镜器械临床前性能验证流程的启动并非随意为之。首先,生产企业需要完成器械的研发和初步设计制造。在这个阶段,企业的研发团队要根据妇科腹腔镜手术的具体需求和临床反馈,确定器械的功能、外形、尺寸等基本参数。例如,根据不同的手术类型,确定抓钳的钳口形状和大小,以适应抓取不同类型病变组织的要求。
接着,企业要组建专门的验证团队。这个团队通常由医疗器械专业人员、工程师、临床医生等多方面人员组成。医疗器械专业人员熟悉各类医疗器械的法规和标准,能够确保验证流程符合相关要求;工程师则负责对器械的物理性能、机械性能等进行测试和分析;临床医生凭借其丰富的临床手术经验,能够从实际使用角度对器械的性能提出宝贵意见。不同专业背景人员的协同合作,为后续全面准确的性能验证奠定了基础。
在启动验证流程之前,还需要明确验证的目标和范围。验证目标要具体明确,比如是验证器械的整体性能,还是侧重于某一项关键性能指标的验证,如电凝钩的电凝效果等。验证范围则要涵盖器械可能涉及的所有使用场景和操作环节,确保在各种可能的情况下器械都能满足性能要求。
四、物理性能验证环节
物理性能验证是妇科腹腔镜器械临床前性能验证的重要组成部分。其中,尺寸精度的验证尤为关键。由于腹腔镜器械需要在狭小的腹腔空间内操作,其尺寸必须精确符合设计要求。例如,穿刺器的外径和长度要精确到毫米级别,否则可能出现穿刺困难或在腹腔内操作不便的情况。验证团队会使用高精度的测量工具,如卡尺等,对器械的各个部位尺寸进行逐一测量,并与设计图纸进行对比,确保偏差在允许范围内。
重量也是一个需要考量的物理性能指标。对于长时间手持操作的器械,如抓钳等,过重的器械会增加医生的操作疲劳感,影响手术效率。因此,需要对器械的重量进行准确测量,并根据临床实际需求设定合理的重量范围。一般来说,轻便且易于操作是理想的状态,在满足器械强度和功能要求的前提下,应尽量减轻器械的重量。
此外,器械的外观表面质量也需要验证。表面应光滑平整,无毛刺、裂纹等缺陷。因为粗糙的表面或存在毛刺的器械可能会对患者的腹腔内组织造成划伤等损伤,而裂纹则可能导致器械在使用过程中发生断裂等严重问题。验证团队会通过目视检查以及使用一些辅助工具,如放大镜等,对器械表面进行细致的检查。
五、机械性能验证环节
机械性能验证对于妇科腹腔镜器械的可靠性至关重要。首先是器械的夹持力验证,以抓钳为例,它需要有足够且稳定的夹持力来抓住病变组织或其他需要操作的物体。验证团队会使用专业的测试设备,模拟临床实际操作时的夹持情况,测量抓钳在不同开合角度下的夹持力大小,并确保其夹持力能够满足临床手术的需求,比如在夹持较硬的组织时不会出现滑脱现象。
转动灵活性也是机械性能验证的一个重要方面。对于腹腔镜镜头、抓钳等可转动的器械,其转动应顺畅无阻,不能出现卡顿或过度松动的情况。验证团队会通过手动转动器械以及使用一些专门的转动测试设备,检查器械的转动性能。如果转动不灵活,在手术中可能会影响医生对器械的操控,导致手术时间延长或操作失误。
再者,器械的开闭性能也需要验证。例如穿刺器的阀门开闭应灵活自如,既能保证在穿刺时防止腹腔内气体泄漏,又能在需要时快速准确地打开或关闭阀门进行相关操作。通过对器械开闭性能的验证,可以确保器械在临床使用过程中能够正常发挥其功能,避免因开闭故障而引发的一系列问题。
六、电气性能验证环节(针对含电气部件器械)
对于部分含有电气部件的妇科腹腔镜器械,如电凝钩、超声刀等,电气性能验证是必不可少的。首先是电绝缘性能的验证。由于这些器械在使用过程中会通过电流,为了防止电流泄漏对患者或操作人员造成电击伤害,必须确保器械具有良好的电绝缘性能。验证团队会使用专业的绝缘电阻测试仪等设备,测量器械的绝缘电阻值,并与标准要求进行对比,确保其绝缘电阻值在规定范围内。
电导率也是一个需要关注的电气性能指标。电凝钩等器械需要通过电流来实现电凝等功能,其电导率要合适,既不能过高导致电流过大造成组织过度损伤,也不能过低影响电凝效果。验证团队会通过专门的电导率测试设备,测量器械的电导率,并根据临床实际需求和标准要求进行调整和验证。
此外,对于电气部件的耐久性也需要进行验证。在多次使用后,电气部件是否还能保持稳定的性能,如电凝钩经过多次电凝操作后,其电凝效果是否依然良好,是否会出现短路等故障。通过模拟临床实际使用情况进行多次重复测试,可以验证电气部件的耐久性,确保其在临床使用过程中能够长期稳定地发挥作用。
七、生物相容性验证环节
生物相容性验证是妇科腹腔镜器械临床前性能验证中关乎患者安全的重要环节。首先是细胞毒性测试,即将器械的提取物与细胞进行培养,观察细胞的生长、存活等情况。如果器械提取物对细胞有明显的毒性作用,那么在临床使用中就可能对患者的组织细胞造成损害。通过细胞毒性测试,可以初步判断器械材料的生物相容性。
致敏性测试也是必不可少的。将器械与动物皮肤或人体志愿者皮肤进行接触,观察是否会引起过敏反应。因为在临床使用中,患者的皮肤或腹腔内组织可能会与器械直接接触,如果器械具有致敏性,就会导致患者出现皮疹、瘙痒等过敏症状,影响患者的健康和手术的顺利进行。
此外,还需要进行植入性测试(对于部分可能在体内留置一段时间的器械)。将器械植入动物体内,观察其在体内的组织反应,如是否会引起炎症、异物反应等。通过植入性测试,可以更全面地了解器械在体内的生物相容性情况,确保其在临床使用中不会对患者的身体造成长期的不良影响。
八、光学性能验证环节(针对有光学部件器械)
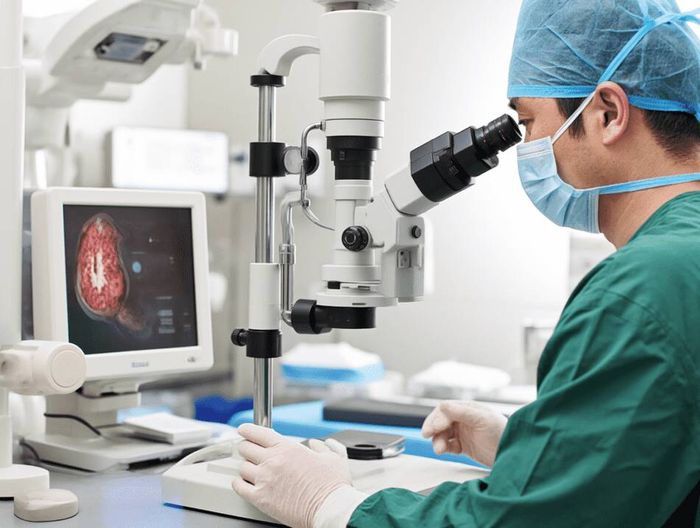
对于带有光学部件的妇科腹腔镜器械,如腹腔镜镜头等,光学性能验证十分重要。首先是成像清晰度的验证。通过将器械对准标准测试图案或实物,观察其成像效果,看是否能够清晰地呈现出图案或实物的细节。成像不清晰的镜头会影响医生对手术部位的观察和判断,可能导致手术失误。验证团队会使用专业的成像测试设备,如分辨率测试仪等,测量镜头的分辨率等参数,以确保其成像清晰度符合临床要求。
色彩还原度也是光学性能验证的一个重要方面。在手术中,准确的色彩还原能够帮助医生更好地辨别不同的组织类型和病变情况。例如,正常的子宫组织和病变的子宫组织在颜色上可能存在差异,如果镜头的色彩还原度不好,医生就难以通过颜色来准确判断组织的状态。验证团队会通过将镜头对准具有不同颜色的测试物体,观察其色彩还原情况,并与真实颜色进行对比,确保其色彩还原度在合理范围内。
此外,光学部件的抗污能力也需要验证。在手术过程中,镜头等光学部件可能会受到血液、组织液等污渍的污染,如果其抗污能力差,就会迅速降低成像清晰度。验证团队会模拟手术中的污染情况,对光学部件进行污染处理,然后观察其恢复成像清晰度的能力,以确保其具有一定的抗污能力,能够在手术过程中保持较好的成像效果。
九、验证结果的评估与记录
在完成妇科腹腔镜器械各项性能验证环节后,需要对验证结果进行全面的评估。评估团队由医疗器械专业人员、临床医生等组成,他们会根据各项性能指标的标准要求,对验证结果进行逐一比对分析。例如,对于物理性能中的尺寸精度验证结果,会看其偏差是否在允许范围内;对于机械性能中的夹持力验证结果,会判断其是否满足临床手术需求等。
评估过程中,要注重对关键性能指标的分析。如果某项关键性能指标未达到标准要求,那么就需要对器械进行进一步的改进或重新设计制造。比如,若电凝钩的电绝缘性能不符合标准,就需要对其电气部件进行重新设计或更换,以确保其符合安全使用的要求。
同时,对验证结果要进行详细的记录。记录内容包括验证的时间、地点、参与人员、各项性能指标的验证结果等。这些记录不仅是对本次验证过程的完整呈现,而且在后续的产品改进、市场准入等方面都具有重要的参考价值。通过规范的记录方式,可以方便日后查询和追溯,确保医疗器械的质量和安全管理的有效性。
热门服务